Dioxyde de cobalt et de lithium
| Dioxyde de cobalt et de lithium | ||
 | ||
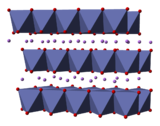 | ||
| Structure du dioxyde de cobalt et de lithium | ||
| Identification | ||
|---|---|---|
| Synonymes | oxyde mixte de cobalt et de lithium | |
| No CAS | 12190-79-3 | |
| No ECHA | 100.032.135 | |
| No CE | 235-362-0 | |
| PubChem | 23670860 | |
| Propriétés chimiques | ||
| Formule | CoLiO2LiCoO2 | |
| Masse molaire[1] | 97,873 ± 0,003 g/mol Co 60,21 %, Li 7,09 %, O 32,69 %, | |
| Précautions | ||
| SGH[2] | ||
 Attention H317 : Peut provoquer une allergie cutanée P280 : Porter des gants de protection/des vêtements de protection/un équipement de protection des yeux/du visage. | ||
| Unités du SI et CNTP, sauf indication contraire. | ||
modifier  | ||
Le dioxyde de cobalt et de lithium, également appelé oxyde mixte de cobalt et de lithium, est le composé chimique de formule LiCoO2. C'est un solide dont la structure a d'abord été calculée de façon théorique avant d'être confirmée notamment par diffraction aux rayons X : cette structure est lamellaire, pouvant être représentée comme des couches d'octaèdres CoO6 d'atomes de cobalt et d'oxygène entre lesquels s'insèrent des atomes de lithium[3].
C'est la structure lamellaire du LiCoO2 qui lui permet de jouer efficacement le rôle de positive dans les accumulateurs au lithium :
- en décharge, la positive se « reconstitue » en fixant des cations Li+ de l'électrolyte qui viennent s'insérer entre les couches d'octaèdres CoO6 en absorbant un électron tandis que des cations Li+ passent en solution dans l'électrolyte du côté de la négative en libérant un électron : ces réactions sont à l'origine de la force électromotrice de ce type d'accumulateurs.
L'oxyde mixte de cobalt et de lithium est toxique en raison du cobalt qu'il contient, et doit être manipulé avec précaution.
Notes et références
- ↑ Masse molaire calculée d’après « Atomic weights of the elements 2007 », sur www.chem.qmul.ac.uk.
- ↑ a et b SIGMA-ALDRICH
- ↑ (en) Yang Shao-Horn, Laurence Croguennec, Claude Delmas, E. Chris Nelson and Michael A. O'Keefem, « Atomic resolution of lithium ions in LiCoO2 », Nature Materials, vol. 2, no 7, , p. 464–467 (DOI 10.1038/nmat922)
v · m | |||
|---|---|---|---|
| Co(0) |
| ||
| Co(II) |
| ||
| Co(II,III) |
| ||
| Co(III) |
| ||
v · m | |
|---|---|
| Inorganiques | |
| Organiques |
|
| Minéraux |
|
 Portail de la chimie
Portail de la chimie










